このスライドは会員限定コンテンツです。
今すぐアカウント登録(無料)して、続きを読みましょう!
1/9
関連するスライド
2022.1.11時点のCOVID治療について
新米ID
22943
136
COVID-19ワクチン UPDATE 2024年度秋冬シーズン
黒田浩一
47421
91
2021.12.22 COVID-19 update
新米ID
6224
24
コロナ禍の発熱外来で遭遇した壊死性筋膜炎について
新米ID
14296
46
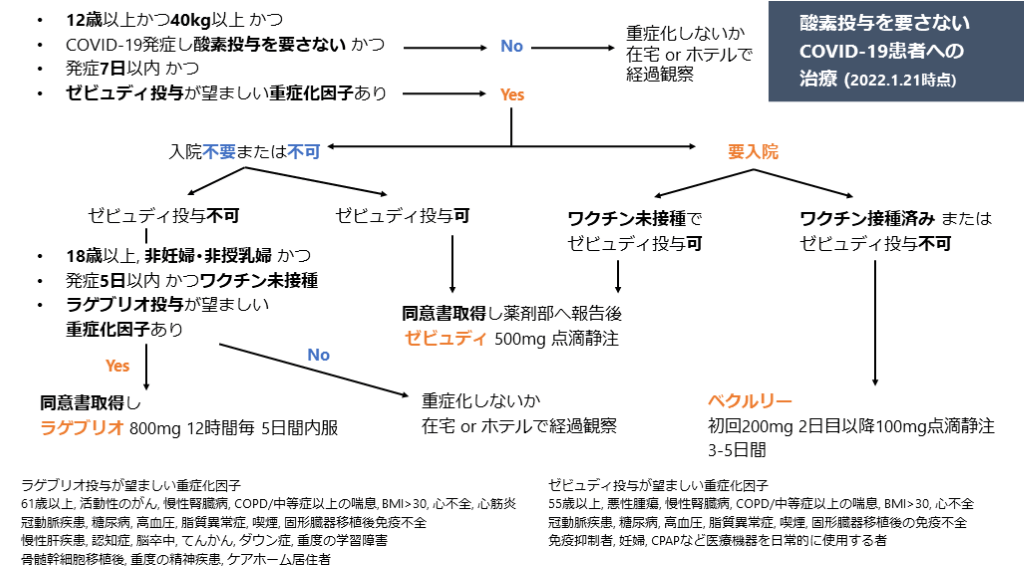
2022.1.23時点の酸素投与を要さない軽症COVIDの治療まとめ
新米ID
Award 2022 受賞者
総合病院鹿児島生協病院
11,432
106
新米IDさんの他の投稿スライド
2026.3.1時点のCOVIDとインフルエンザのまとめ
新米ID
2,133,800
6,629
2022.1.11時点のCOVID治療について
新米ID
22,943
136
2022.12.30更新 細菌感染症の治療期間まとめ
新米ID
101,297
977
このスライドと同じ診療科のスライド
会員登録・ログインで「スライド内のテキスト」を参照いただけます。